Elinext a développé une plateforme logicielle modulaire qui permet aux entreprises des sciences de la vie de rationaliser l'exécution et la commercialisation des essais cliniques mondiaux et de collaborer sur des partenariats tout en réduisant les charges administratives.
Défis
Avant de s'adresser à Elinext, l'entreprise utilisait une solution obsolète basée sur la plateforme Domino et l'ancienne version d'ExtJS. L'application a été entièrement refactorisée pour utiliser une plateforme Origami moderne avec la dernière version d'ExtJS.
L'objectif principal du système était de simplifier les tâches associées à la gestion des documents.
Solution
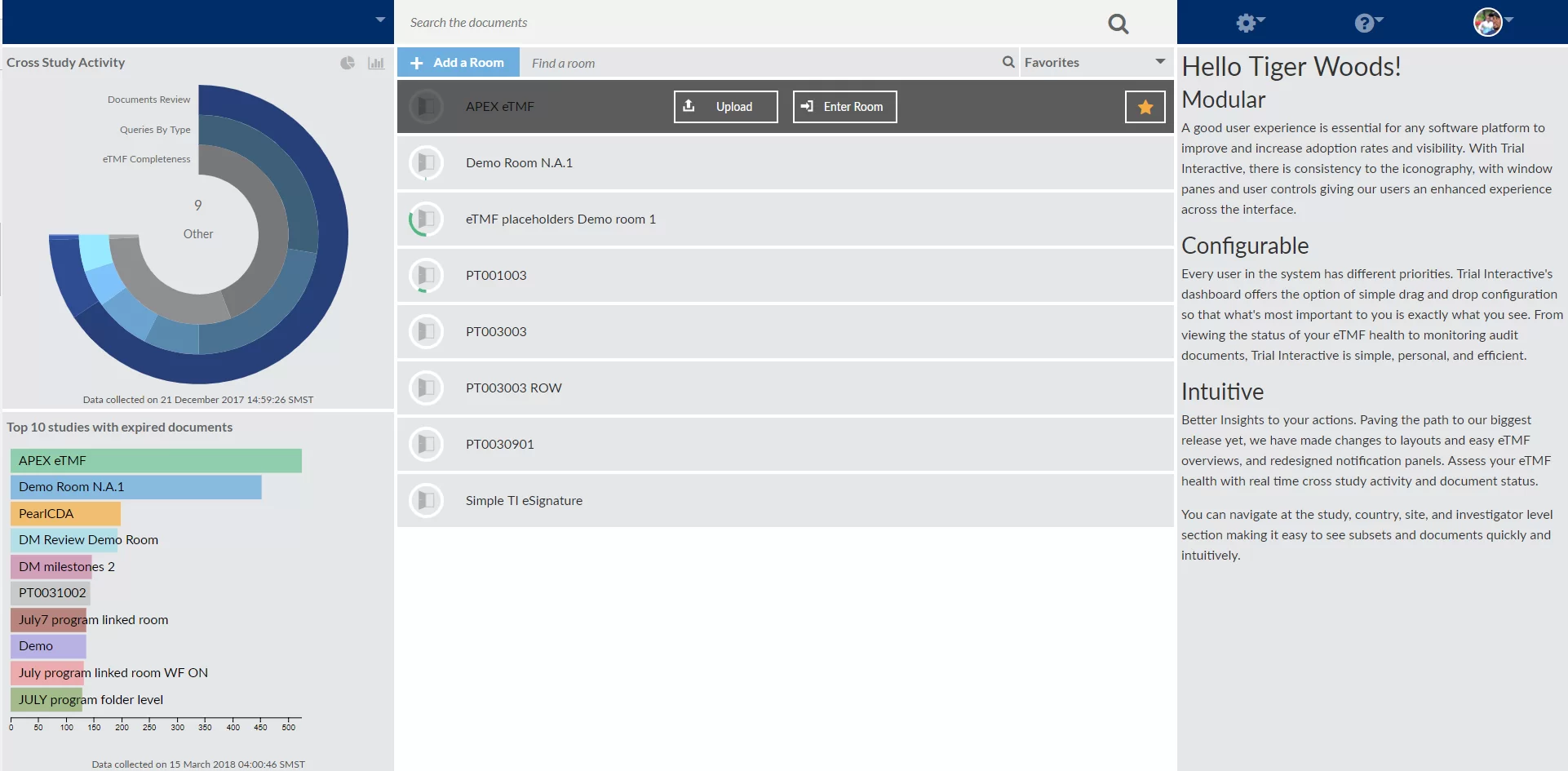
Depuis 2010, l'équipe d’Elinext a développé la plateforme SaaS complète pour la gestion des essais cliniques et la collaboration avec une interface modulaire configurable et l'hébergement sécurisé des fichiers dans un entrepôt de données virtuel centralisé compatible avec la norme 21 CFR Partie 11.
Au cours du travail, l'équipe a travaillé sur les modules suivants:
Panneau de super-administrateur (pour les ingénieurs de support - peut être externalisé à la société pharmaceutique cliente):- configuration d'instance de haut niveau;
- activer / désactiver les modules.
- paramètres généraux;
- gestion des utilisateurs et des groupes;
- configuration pour la sécurité des documents;
- configuration du flux de travail;
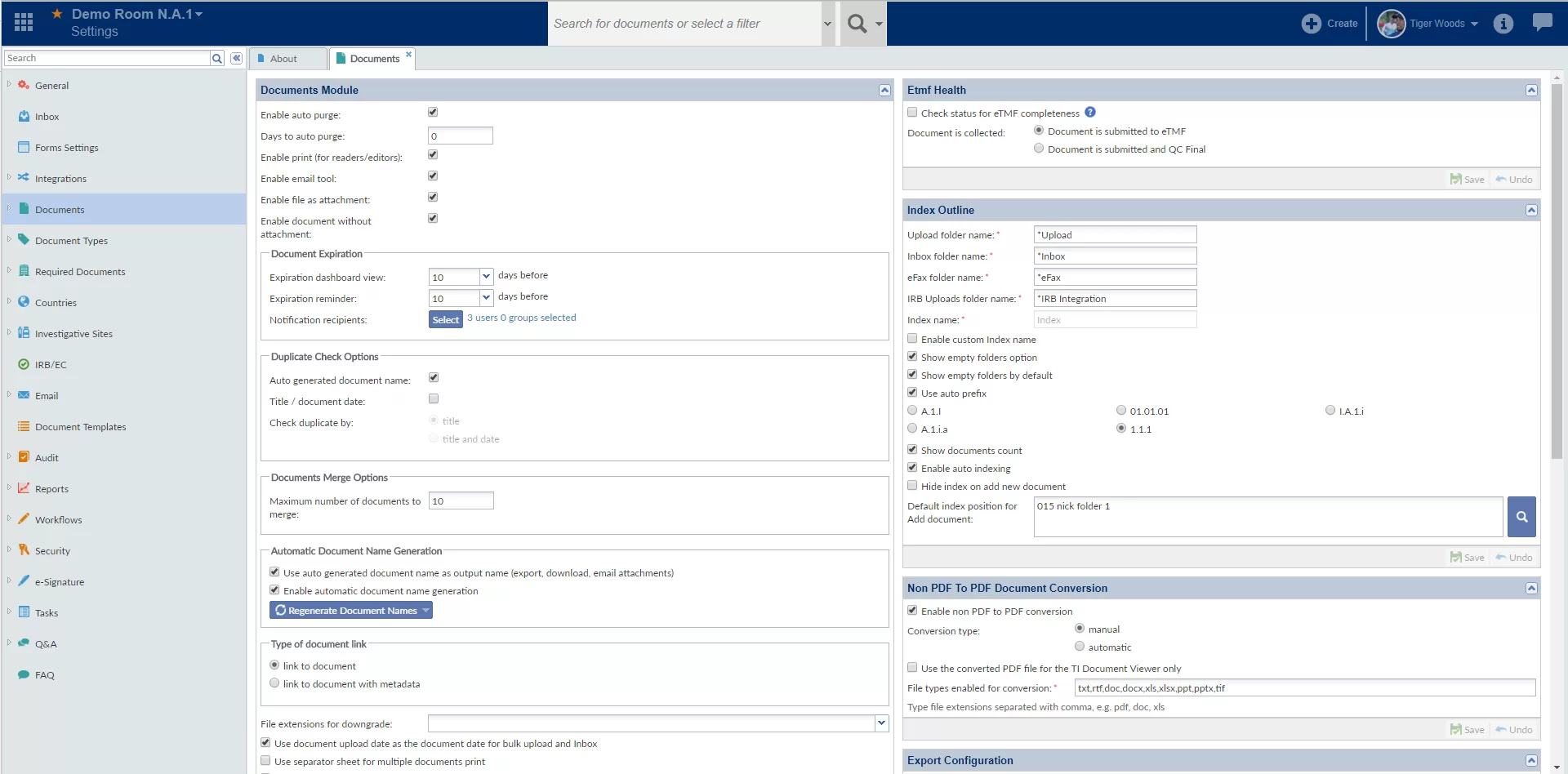
- configuration de la gestion des documents;
- configuration des études eTMF;
- configuration des rapports;
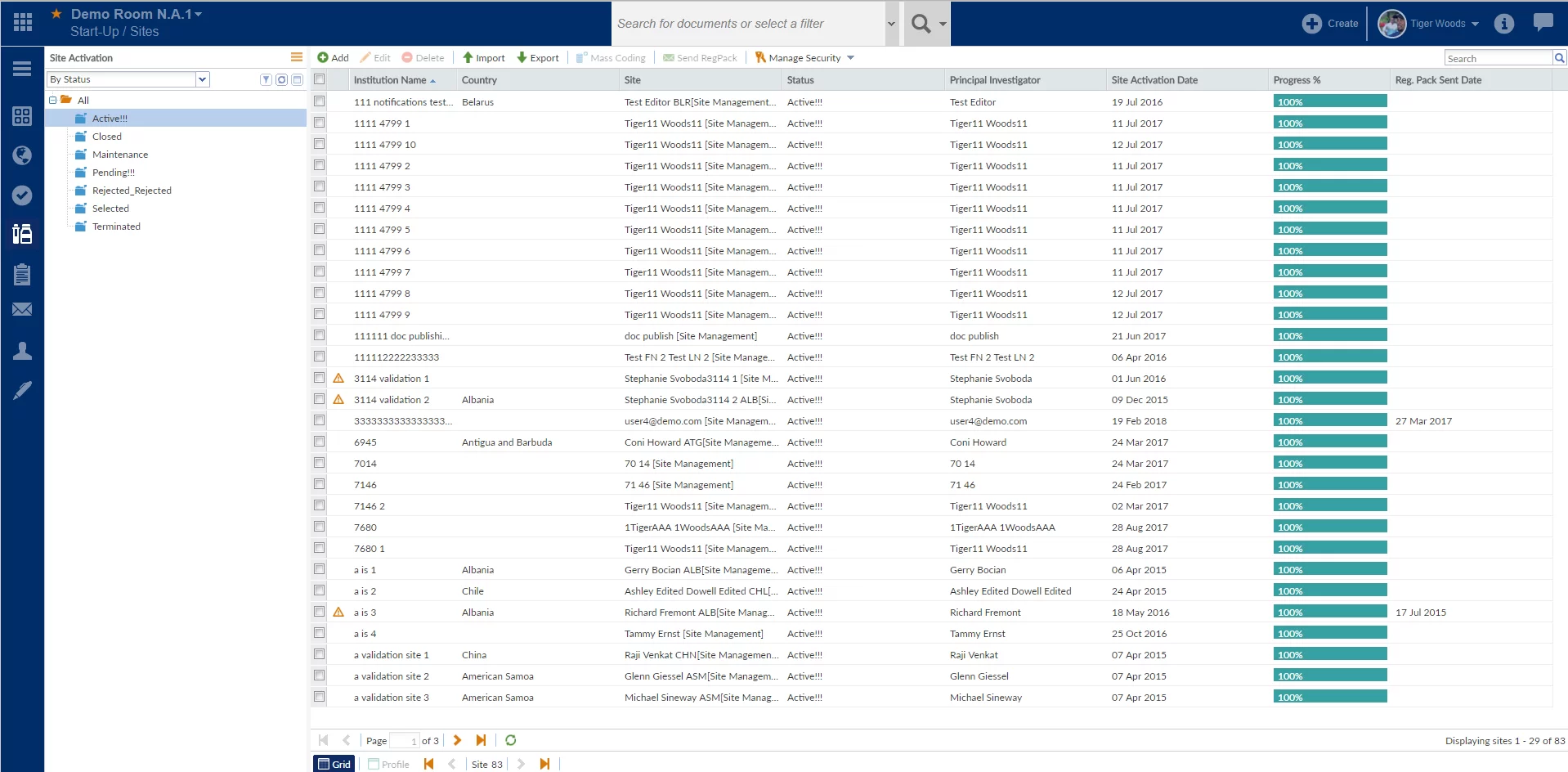
- configuration des sites d'investigation;
- configuration de démarrage de l'étude.
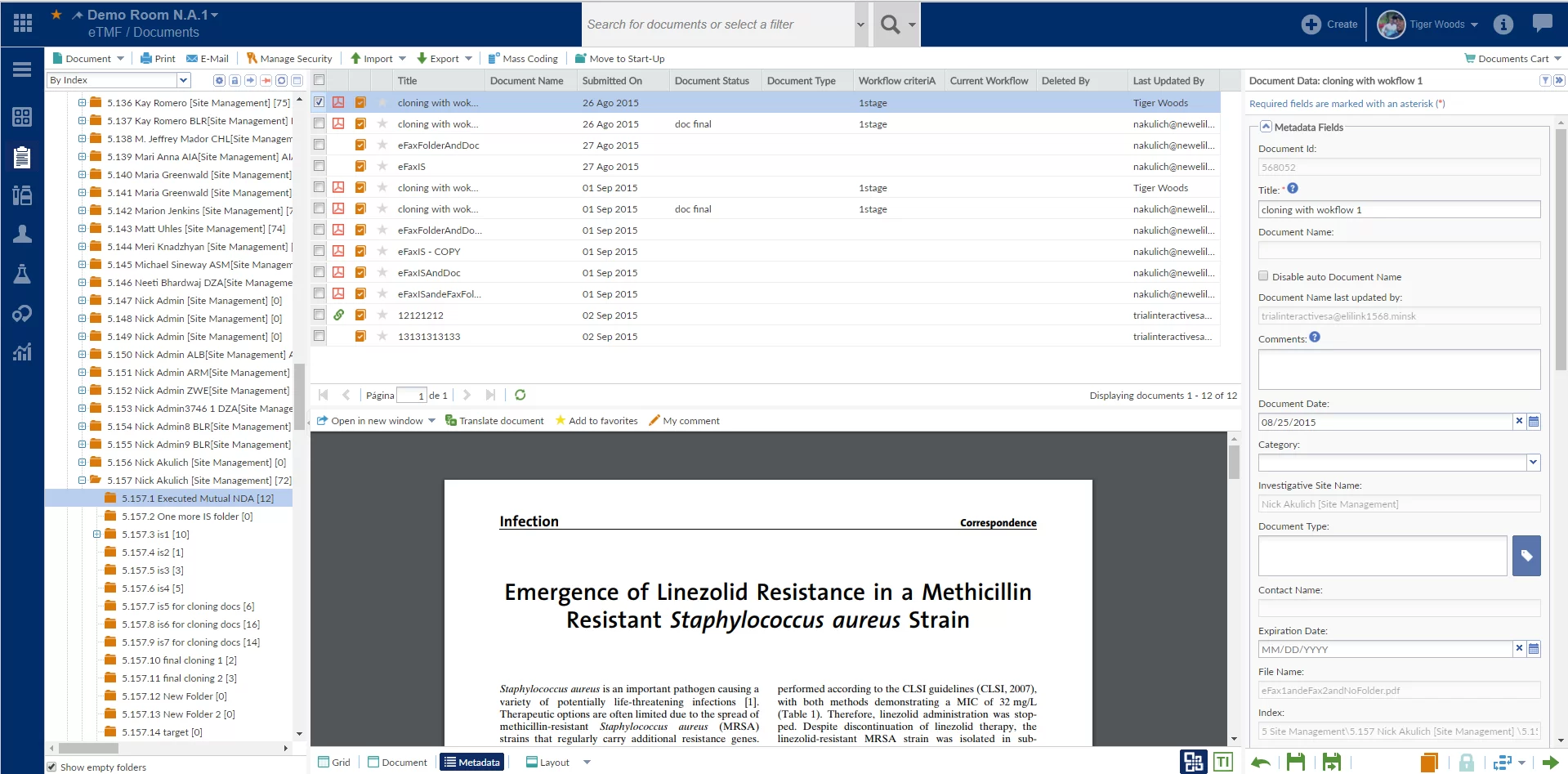
- gestion des documents;
- codage des métadonnées;
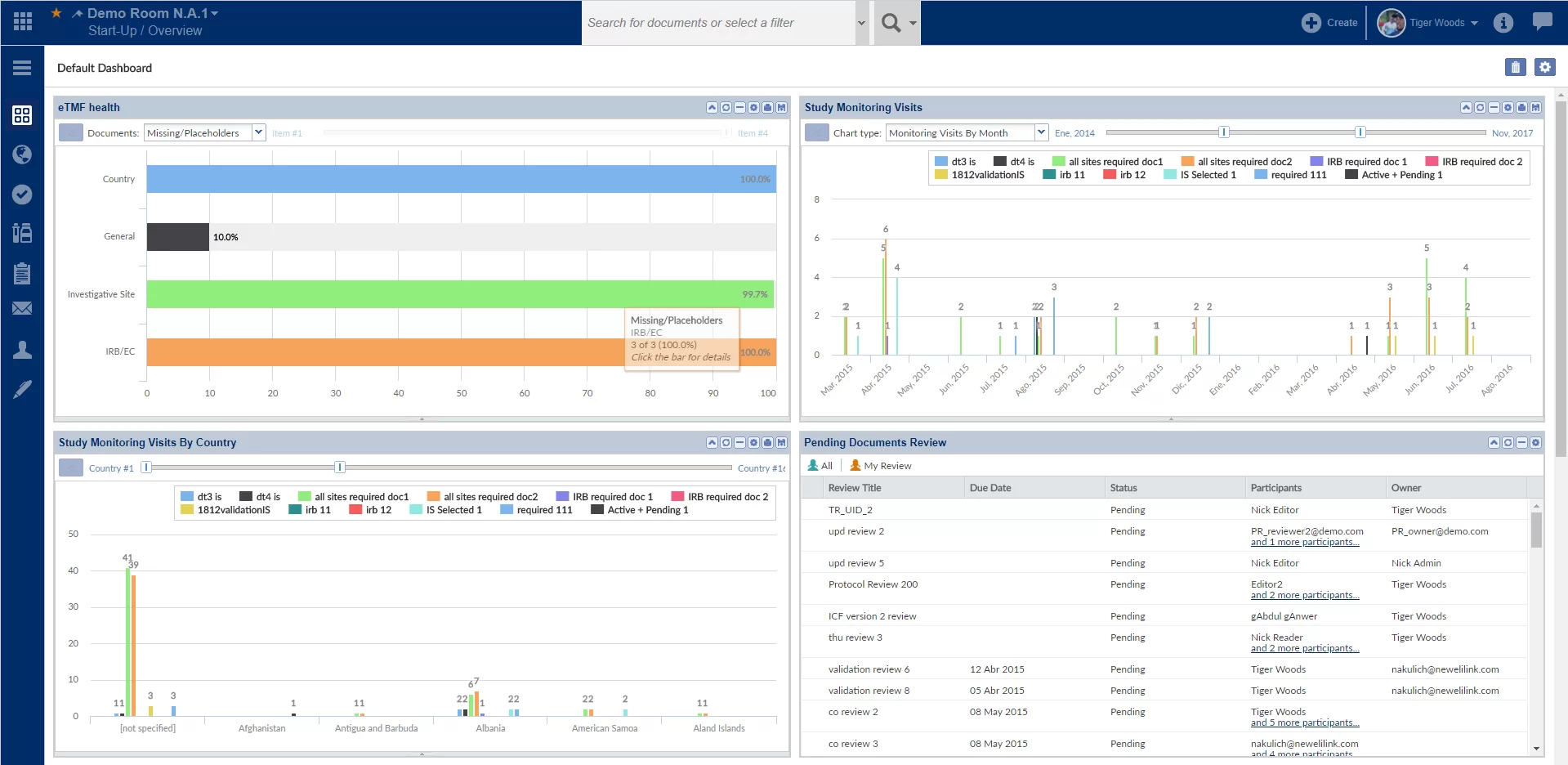
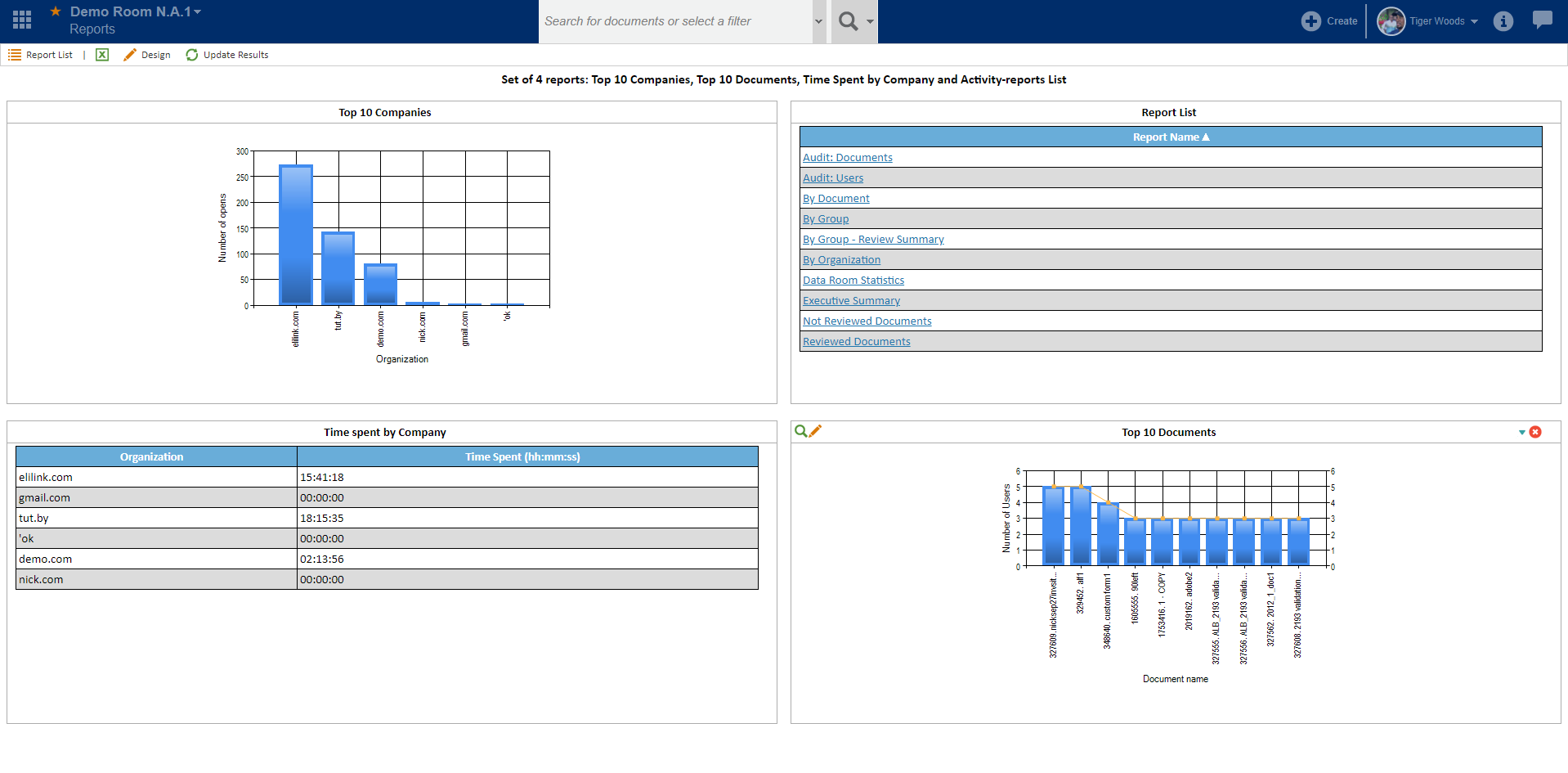
- rapports et tableaux de bord;
- gestion des tâches;
- audit;
- communication;
- Q&A.
De plus, l'équipe a mis en œuvre tous les tableaux de bord et métriques pour examiner la tenue des essais cliniques avec des schémas, des graphiques et des diagrammes. En utilisant un module de rapport, on peut auditer n'importe quelle activité pour une étude spécifique.
Plusieurs documents peuvent être importés en même temps à l'aide des archives Windows – auparavant, cela a été fait un par un. En outre, on peut exporter des documents vers une archive ou exporter les métadonnées des documents vers des fichiers HTML, EXCEL ou WORD.
Pour répondre aux normes de haute qualité de l'industrie pharmaceutique, notre équipe a mis en place le processus d'assurance qualité à partir de zéro, mis en œuvre des méthodologies de développement Agile, des tests manuels, automatisés et de charge. Au total, plus de 5 000 tests manuels et 2 100 tests automatisés ont été effectués, plus de 5 000 défauts ont été détectés et documentés.
Le système est déployé sur 150 serveurs et compte plus de 50 000 utilisateurs. La préparation et l'audit de la documentation de test sont conformes aux normes 21 CFR Partie 11.
Spécificités- Gestion de la sécurité des documents par signature électronique - chaque utilisateur disposant des droits appropriés peut consulter le document avec certaines restrictions pour l'enregistrement, la copie, etc. et signer si nécessaire.
- Reconnaissance automatique d'un type de document.
- Migration des modules d'une solution basée sur ExtJS vers Angular.
- Intégration de nombreux modules tiers: IRB/EC utilisant des API, eSignature, Alfresco,
- Sharepoint, DocuSign, Adlib, PleaseReview, AbobeSign, Seclore, Snowbound viewer, ARender viewer, Prizm viewer.
- Intégration étendue avec le tout nouveau système CMS Alfresco, préservant toutes les fonctions et les avantages.
Résultats
Le résultat du projet est une solution SaaS robuste avec une architecture complètement nouvelle. La solution est utilisée par les sociétés pharmaceutiques, biotechnologiques et de dispositifs médicaux, ainsi que par les ORC, les IRB/ECs et les principaux instituts universitaires de développement clinique.
Les ingénieurs d'Elinext continuent d'ajouter de nouvelles fonctionnalités au système pour répondre à toutes les normes élevées des essais cliniques.